| Jewiki unterstützen. Jewiki, die größte Online-Enzyklopädie zum Judentum.
Helfen Sie Jewiki mit einer kleinen oder auch größeren Spende. Einmalig oder regelmäßig, damit die Zukunft von Jewiki gesichert bleibt ... Vielen Dank für Ihr Engagement! (→ Spendenkonten) |
How to read Jewiki in your desired language · Comment lire Jewiki dans votre langue préférée · Cómo leer Jewiki en su idioma preferido · בשפה הרצויה Jewiki כיצד לקרוא · Как читать Jewiki на предпочитаемом вами языке · كيف تقرأ Jewiki باللغة التي تريدها · Como ler o Jewiki na sua língua preferida |
Polycaprolactam
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|

| |||||||
| Allgemeines | |||||||
| Name | Polycaprolactam | ||||||
| Andere Namen |
| ||||||
| CAS-Nummer | 25038-54-4 | ||||||
| Monomer | Caprolactam | ||||||
| Summenformel der Wiederholeinheit | C6H11NO | ||||||
| Molare Masse der Wiederholeinheit | 113,16 g·mol−1 | ||||||
| PubChem | 32775 | ||||||
| Art des Polymers | |||||||
| Eigenschaften | |||||||
| Aggregatzustand |
fest | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Polycaprolactam (Polyamid 6, PA6, als Handelsmarke Perlon) ist ein Polymer aus der Gruppe der Polyamide. Dieses Polymer wurde erstmals 1938 von Paul Schlack (I.G. Farben) synthetisiert, um die Eigenschaften von Nylon 6,6 zu reproduzieren, ohne das geltende Produktionspatent zu verletzen.
Herstellung
Polyamid 6 entsteht durch ringöffnende Polymerisation von ε-Caprolactam.
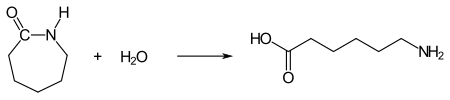
Hydrolytische Kettenpolymerisation: Für die Startreaktion wird ε-Aminocapronsäure benötigt. Sie wird durch hydrolytische Ringöffnung aus ε-Caprolactam gewonnen. Dazu werden geringe Mengen an Wasser zugesetzt:
ε-Aminocapronsäure reagiert zusammen mit ε-Caprolactam unter Ausbildung von Amidbindungen zum Polycaprolactam:
Die Kettenpolymerisation erfolgt unter Ringöffnung an die Amino-Endgruppe der wachsenden Kette.[2] In kontinuierlichen (VK-Rohr-Verfahren) oder diskontinuierlichen Verfahren erfolgt die Reaktionen im Bereich von 260 bis 280 °C (VK-Rohr-Verfahren: 240 °C). Die Reaktionszeit beträgt 8 bis 10 Stunden. Verbleibende Monomere werden aus der Schmelze des Produkts im Vakuum entgast oder aus dem Granulat mit Wasser extrahiert.[3]
Anionische Kettenpolymerisation: Diese Polymerisation verläuft vergleichsweise kompliziert.[4] Zur Initiierung wird ε-Caprolactam mit Alkoholaten, primären oder sekundären Aminen in ein Anion überführt.
Es entsteht nach Addition von Caprolactam ein N-acyliertes Caprolactam, das eigentliche aktive Kettenende der Kettenwachstumsreaktion. Die Wachstumsreaktion erfolgt nach:
Die langsam verlaufende Bildung von aktiven Kettenenden kann mit Carbonsäurechloriden, Anhydriden oder Isocyanaten beschleunigt werden:
Unter Stickstoffatmosphäre erfolgt die exotherme Kettenpolymerisation bei 120 bis 150 °C innerhalb weniger Minuten.[3]
Polykondensation: Die Synthese von Polyamid 6 ist auch über eine Polykondensation von ε-Aminocapronsäure möglich:
Verwendung
Polycaprolactam findet als Kunstfaser unter dem Namen Perlon Verwendung.[5] Eine Vielzahl gegossener (PA6G) und extrudierter (PA6E) Bauteile werden aus Polycaprolactam hergestellt. Der Kunststoff wird auf Grund der Zähigkeit und Verschleißfestigkeit im Maschinenbau für gering belastete Zahnräder und Schrauben, sowie wegen der guten Gleiteigenschaften für hoch belastete Gleitlager und -platten verwendet.[6]
In der Dünnschicht- und Säulenchromatographie wird es als Trägermaterial (stationäre Phase) verwendet.[7]
Einzelnachweise
- ↑ Diese Substanz wurde in Bezug auf ihre Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Bernd Tieke, Makromolekulare Chemie, 3. Auflage, Wiley-VCH, Weinheim, 2014, S. 117.
- ↑ 3,0 3,1 Wolfgang Kaiser, Kunststoffchemie für Ingenieure, 3. Auflage, Carl Hanser, München, 2011, S. 363.
- ↑ Bernd Tieke, Makromolekulare Chemie, 3. Auflage, Wiley-VCH, Weinheim, 2014, S. 112f.
- ↑ Karl-Heinz Lautenschläger, Werner Schröter: Taschenbuch der Chemie, Harri Deutsch Verlag, 2007, Google Books (Link nicht mehr abrufbar).
- ↑ EUROPA Tabellenbuch Metall.
- ↑ Der BibISBN-Eintrag Vorlage:BibISBN/9783540922056 ist nicht vorhanden. Bitte prüfe die ISBN und lege ggf. einen neuen Eintrag an.
| Dieser Artikel basiert ursprünglich auf dem Artikel Polycaprolactam aus der freien Enzyklopädie Wikipedia und steht unter der Doppellizenz GNU-Lizenz für freie Dokumentation und Creative Commons CC-BY-SA 3.0 Unported. In der Wikipedia ist eine Liste der ursprünglichen Wikipedia-Autoren verfügbar. |