| Jewiki unterstützen. Jewiki, die größte Online-Enzyklopädie zum Judentum.
Helfen Sie Jewiki mit einer kleinen oder auch größeren Spende. Einmalig oder regelmäßig, damit die Zukunft von Jewiki gesichert bleibt ... Vielen Dank für Ihr Engagement! (→ Spendenkonten) |
How to read Jewiki in your desired language · Comment lire Jewiki dans votre langue préférée · Cómo leer Jewiki en su idioma preferido · בשפה הרצויה Jewiki כיצד לקרוא · Как читать Jewiki на предпочитаемом вами языке · كيف تقرأ Jewiki باللغة التي تريدها · Como ler o Jewiki na sua língua preferida |
Kanamycine
Die Kanamycine sind eine Gruppe strukturell eng verwandter Glycoside. In allen Fällen ist das 2-Desoxystreptamin (mittlerer Teil in der Struktur) glycosidisch über die 4–OH-Gruppe an ein 3-D-Glucosaminderivat verknüpft.
Handelsübliches Kanamycin enthält hauptsächlich Kanamycin A, ist aber ein Gemisch aus den Kanamycinen A, B und C. Es ist ein verschreibungspflichtiges Aminoglycosid-Antibiotikum aus Streptomyceten (Streptomyces kanamyceticus).
Tobramycin ist strukturell mit den Kanamycinen eng verwandt. Es kann aus Kanamycin B synthetisiert oder alternativ aus Fermentationslösungen von Streptomyces tenebarius gewonnen werden.[1] Tobramycin ist ein gut geeignetes Aminoglycosidantibiotikum zur Behandlung von Pseudomonas aeruginosa-Infektionen. Dabei kommt Tobramycin sowohl als intravenöse Kurzinfusion (30–60min) als auch bei Mukoviszidose-Patienten mit einer Pseudomonas aeruginosa-Besiedlung in Form einer Inhalations-Therapie zum Einsatz.
Eigenschaften
Kanamycine sind basische, stark polare Oligosaccharide. Sie sind farblos, gut wasserlöslich und im pH-Bereich von 2,2–10,0 lösungsstabil.
| Kanamycine | ||||||||||
| Name | Kanamycin A | Kanamycin B | Kanamycin C | Tobramycin | Dibekacin | |||||
| Strukturformel | 
|

|
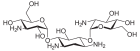
|

|
||||||
| CAS-Nummer | 8063-07-8 64013-70-3 (Disulfat) |
4696-76-8 | 2280-32-2 | 32986-56-4 | 34493-98-6 | |||||
| PubChem | 6032 | 439318 | 439582 | 36294 | 470999 | |||||
| Summenformel | C18H36N4O11 | C18H37N5O10 | C18H36N4O11 | C18H37N5O9 | C18H37N5O8 | |||||
| Molare Masse | 484,50 g·mol−1 | 483,52 g·mol−1 | 484,50 g·mol−1 | 467,52 g·mol−1 | 451,52 g·mol−1 | |||||
| Aggregatzustand | fest | |||||||||
| GHS- Kennzeichnung |
Disulfat |
Sulfat
|
|
|
| |||||
| H- und P-Sätze | 360 | keine H-Sätze | siehe oben | keine H-Sätze | siehe oben | |||||
| keine EUH-Sätze | keine EUH-Sätze | siehe oben | keine EUH-Sätze | siehe oben | ||||||
| 201‐308+313 | siehe oben | siehe oben | keine P-Sätze | siehe oben | ||||||
| Toxikologische Daten | > 4000 mg·kg−1 (LD50, Ratte, oral)[5] | > 7500 mg·kg−1 (LD50, Ratte, oral)[6] | ||||||||
Verwendung
In Deutschland wird Kanamycin in der Humanmedizin als Sulfatsalz in Form von Augentropfen und -salben zur lokalen Behandlung bakterieller Infektionen des Auges (z. B. bei einer Bindehautentzündung) eingesetzt. In den USA sind von Kanamycin auch Darreichungsformen zur oralen und parenteralen Anwendung (Kantrex®) im Handel.
In der Veterinärmedizin wird Kanamycin als Reserveantibiotikum zur Behandlung von Magen-Darm-Infektionen durch Kanamycin-empfindliche Erreger bei Hunden und Katzen sowie in Kombination mit Spiramycin bei akuten und chronischen, gegen andere Therapien resistente Mastitiden verwendet. In der Humanmedizin dient Kanamycin als Reserveantibiotikum unter anderem für die Behandlung multiresistenter Tuberkulose.
Weit verbreitet ist es auch in der Molekularbiologie als Selektionsantibiotikum. Gentechnisch veränderte Mikroorganismen, vornehmlich Escherichia coli werden zusätzlich zu den interessierenden Genen mit Resistenzgenen gegen Kanamycin ausgestattet. Somit wird eine Auslese von veränderten gegenüber nativen Mikroorganismen erlaubt, indem man in kanamycinhaltigen Medien kultiviert. Um solche transgenen E. coli Bakterien beispielsweise in LB-Medium selektiv zu kultivieren, wird eine Endkonzentration von etwa 50 µg/ml Medium verwendet. Auch andere Antibiotika wie Ampicillin oder Tetracycline werden für Selektionsmedien eingesetzt.
Im Gegensatz zu den meisten anderen Antibiotika wirkt Kanamycin auch auf Pflanzen toxisch. Entsprechend kann beim Arbeiten mit transgenen Pflanzen und einer entsprechenden Versuchsdurchführung auch auf Kanamycin-Selektionsmedien zurückgegriffen werden.
Wirkungsweise
Kanamycin durchdringt die bakteriellen Zellmembranen durch passive Diffusion oder durch (sauerstoffabhängigen) aktiven Transport. Es lagert sich an die 30S-Untereinheit membranassoziierter Ribosomen an und hemmt damit die bakterielle Proteinsynthese.
Analytik
Zur zuverlässigen Bestimmung eignet sich nach angemessener Probenvorbereitung die Kopplung der HPLC mit der Massenspektrometrie.[7][8][9] Auch Immunassays können eingesetzt werden.[10]
Handelsnamen
- Kanamycin-Monopräparate
Kanamycin ist in Deutschland unter den folgenden Namen erhältlich:
- zur topischen Anwendung (Augensalbe/-tropfen):
- KANAMYCIN-POS
- KANAMYTREX
- Tobramycin-Monopräparate
Tobramycin ist in Deutschland unter den folgenden Namen erhältlich:
- zur Inhalation bei Mukoviszidose:
- TOBI
- BRAMITOB
- GERNEBCIN
- zur topischen Anwendung (Salbe):
- TOBRAMAXIN
- zur parenteralen Anwendung
- Tobramycin B. Braun
- GERNEBCIN
- TobraZid
Einzelnachweise
- ↑ Theodor Dingermann, Rudolf Hänsel, Ilse Zündorf (Hrsg.): Pharmazeutische Biologie: Molekulare Grundlagen und klinische Anwendungen. 1. Auflage. Springer Verlag, Berlin 2002, ISBN 3-540-42844-5, S. 309 ff.
- ↑ Datenblatt Kanamycin disulfate salt from Streptomyces kanamyceticus bei Sigma-Aldrich, abgerufen am 3. Mai 2011 (PDF).
- ↑ Datenblatt Kanamycin B sulfate salt bei Sigma-Aldrich, abgerufen am 3. Mai 2011 (PDF).
- ↑ Datenblatt Tobramycin bei Sigma-Aldrich, abgerufen am 3. Mai 2011 (PDF).
- ↑ Eintrag zu Kanamycine in der DrugBank der University of Alberta.
- ↑ Vorlage:Calbiochem
- ↑ J. A. Dijkstra, M. G. Sturkenboom, K. v. Hateren, R. A. Koster, B. Greijdanus, J. W. Alffenaar: Quantification of amikacin and kanamycin in serum using a simple and validated LC-MS/MS method. In: Bioanalysis. 6(16). Aug 2014, S. 2125–2133. PMID 25331857
- ↑ Q. Gong, L. Ding, S. Zhu, Y. Jiao, J. Cheng, S. Fu, L. Wang: Determination of ten aminoglycoside residues in milk and dairy products using high performance liquid chromatography-tandem mass spectrometry. In: Se Pu. 30(11), Nov 2012, S. 11437. PMID 23451516 (chinesisch)
- ↑ P. Kumar, A. Rúbies, R. Companyó, F. Centrich: Determination of aminoglycoside residues in kidney and honey samples by hydrophilic interaction chromatography-tandem mass spectrometry. In: J Sep Sci. 35(20), Okt 2012, S. 2710–2717. PMID 23065931
- ↑ J. A. Dijkstra, A. J. Voerman, B. Greijdanus, D. J. Touw, J. W. Alffenaar: Immunoassay Analysis of Kanamycin in Serum Using the Tobramycin Kit. In: Antimicrob Agents Chemother. 60(8), 22. Jul 2016, S. 4646–4651. PMID 27185806
| Dieser Artikel basiert ursprünglich auf dem Artikel Kanamycine aus der freien Enzyklopädie Wikipedia und steht unter der Doppellizenz GNU-Lizenz für freie Dokumentation und Creative Commons CC-BY-SA 3.0 Unported. In der Wikipedia ist eine Liste der ursprünglichen Wikipedia-Autoren verfügbar. |