| Jewiki unterstützen. Jewiki, die größte Online-Enzyklopädie zum Judentum.
Helfen Sie Jewiki mit einer kleinen oder auch größeren Spende. Einmalig oder regelmäßig, damit die Zukunft von Jewiki gesichert bleibt ... Vielen Dank für Ihr Engagement! (→ Spendenkonten) |
How to read Jewiki in your desired language · Comment lire Jewiki dans votre langue préférée · Cómo leer Jewiki en su idioma preferido · בשפה הרצויה Jewiki כיצד לקרוא · Как читать Jewiki на предпочитаемом вами языке · كيف تقرأ Jewiki باللغة التي تريدها · Como ler o Jewiki na sua língua preferida |
Röteln
| Klassifikation nach ICD-10 | ||
|---|---|---|
| B06.0 | Röteln mit neurologischen Komplikationen | |
| B06.8 | Röteln mit sonstigen Komplikationen | |
| B06.9 | Röteln ohne Komplikation | |
| ICD-10 online (WHO-Version 2013) | ||
Die Röteln (Rubella) sind eine hochansteckende Infektionskrankheit, die durch das Rötelnvirus ausgelöst wird und eine lebenslange Immunität hinterlässt, weshalb sie zu den Kinderkrankheiten zählen. Rötelnviren befallen nur Menschen. Neben den typischen roten Hautflecken (Exanthem) können auch Fieber und Lymphknotenschwellungen auftreten. Gefürchtet ist eine Rötelninfektion während der Schwangerschaft, weil sie zu schweren Komplikationen (Rötelnembryofetopathie) mit ausgeprägten Fehlbildungen des Kindes und zu Fehlgeburten führen kann. Die Behandlung besteht in rein symptomatischen Maßnahmen (Linderung der Krankheitssymptome). Eine vorbeugende Lebendimpfung ist verfügbar.[1][2] Die Erkrankung an Röteln sowie der labordiagnostische Nachweis sind mit der Änderung des Infektionsschutzgesetzes vom 29. März 2013 meldepflichtig geworden.[3]
Verbreitung
Das Rötelnvirus ist – mit dem Menschen als einzigem Wirt – weltweit verbreitet. In Bevölkerungsgruppen mit einer niedrigen Durchimpfungsrate erfolgen 80–90 % der Infektionen im Kindesalter. In Deutschland bestand bis März 2013 nur in den neuen Bundesländern eine Meldepflicht, danach im ganzen Bundesgebiet. So kann vor März 2013 die aktuelle Verbreitung nur hochgerechnet werden. Aus den in Deutschland gemeldeten Zahlen ergab sich für das Jahr 2003 eine Inzidenz von 0,33 Fällen pro 100.000 Einwohnern.[4] Das Europäische Zentrum für die Prävention und die Kontrolle von Krankheiten hat von Oktober 2011 bis September 2012 aus 26 Ländern über 30.000 Infektionen erfasst mit den höchsten Inzidenzen in Rumänien (114,32/100.000) und Polen (13,93/100.000). Die durchschnittliche Inzidenz aller 26 Länder lag bei 8,6/100.000.[5] Bei Schuleingangsuntersuchungen in Deutschland von 2010 waren 91,2 % der Kinder vollständig geimpft.[6] Die unvollständige Durchimpfung der Bevölkerung kann zu sporadischen und epidemischen Infektionen bei Kindern, Jugendlichen und auch Erwachsenen führen. Selektive Impfungen von jungen Mädchen und Frauen ab dem 13. Lebensjahr – bedingt durch die besondere Gefahr dieser Krankheit während einer Schwangerschaft – haben in der weiblichen Bevölkerung erreicht, dass die bei der natürlichen Durchseuchung noch bestehenden Immunitätslücken im jungen Erwachsenenalter zunehmend besser geschlossen wurden. Eine angeborene Rötelninfektion wurde in den Jahren 2010 und 2011 nicht mehr gemeldet.[7] Allerdings geht das Robert-Koch-Institut von einer erheblichen Untererfassung aus, weil es Hinweise darauf gibt, dass nur erkennbar geschädigte Neugeborene untersucht und gemeldet werden. Wahrscheinlich entgehen Fälle mit erst später erkennbaren Folgen einer Rötelninfektion während der Schwangerschaft der Erfassung und Meldung.[4]
Weltweit dagegen wird von über 100.000 Kindern ausgegangen, die jedes Jahr mit einer Rötelnembryofetopathie geboren werden.[8]
Erreger
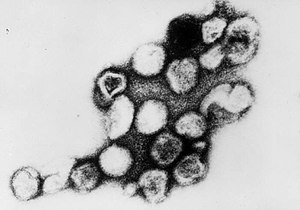
Das Rötelnvirus ist das einzige Mitglied der Gattung Rubivirus und gehört zur Familie der Togaviridae, deren Mitglieder typischerweise eine einzelsträngige RNA mit positiver Polarität als Genom besitzen, das von einem ikosaedrischen Kapsid umgeben ist. Das RNA-Genom im Inneren des Kapsids hat eine Länge von ungefähr 9.757 Nukleotiden und codiert für zwei nichtstrukturelle Proteine sowie drei strukturelle Proteine.[9] Das Kapsidprotein sowie die beiden Hüllproteine E1 und E2 machen die drei strukturellen Proteine aus.
Die kugelförmigen Viruspartikel der Togaviridae haben einen Durchmesser von 50–70 nm und sind von einer Lipidmembran (Virushülle) umgeben. In der Hülle sind als deutliche Spikes (Ausstülpungen) von 6 nm Höhe die Heterodimere der beiden viralen Hüllproteine E1 und E2 eingelagert.[10] Es existiert eine einheitliche Form der Oberflächenstruktur, also nur ein einziger Serotyp.[1]
Übertragung
Die Übertragung erfolgt durch eine Tröpfcheninfektion mit 50-prozentiger Kontagiosität. Die Inkubationszeit beträgt 14–21 Tage. Eine Woche vor bis eine Woche nach Ausbruch des Exanthems ist der Patient ansteckend.[1] Die Viren dringen über die Schleimhäute der oberen Atemwege ein und werden zunächst bevorzugt in lymphatischem Gewebe vermehrt. Anschließend erfolgt eine Ausschüttung in die Blutbahn (Virämie). Im Falle einer Schwangerschaft kann eine Übertragung des Virus über den Mutterkuchen (Plazenta) auf das ungeborene Kind erfolgen.[1]
Krankheitserscheinungen
Der Verlauf der Erkrankung ist von Mensch zu Mensch sehr unterschiedlich und nicht sehr spezifisch, das heißt leicht mit anderen fieberhaften Erkrankungen mit Hautausschlag verwechselbar. In etwa der Hälfte der Infektionen treten überhaupt keine Symptome auf (asymptomatischer Verlauf, stille Feiung).[1]
Typische Symptomatik
Nach der Inkubationszeit können sich zunächst im Gesicht gerötete, einzelstehende, leicht erhabene Flecken (Effloreszenzen) bilden, die sich auf den Rumpf und die Extremitäten ausbreiten. Diese bilden sich meist nach ein bis drei Tagen zurück. Begleitend tritt oft erhöhte Temperatur bis 39 °C auf. Hinzu kommen eventuell Kopf- und Gliederschmerzen, eine Lymphknotenschwellung an Hinterkopf, Nacken und hinter den Ohren sowie ein leichter Katarrh der oberen Luftwege und eine Bindehautentzündung[1].
Komplikationen
Seltene, mit zunehmendem Lebensalter des Patienten häufiger werdende Komplikationen sind Gelenkentzündungen (Arthritis), eine Verringerung der Zahl der Blutplättchen (Thrombozytopenie) mit vermehrter Blutungsneigung oder eine Enzephalitis. Darüber hinaus kann es auch zu einer Bronchitis, einer Mittelohrentzündung oder einer Herzbeteiligung (Myo- und Perikarditis) kommen.[1]
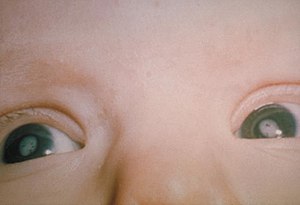
Eine besondere Gefahr stellt jedoch eine Rötelninfektion während einer Schwangerschaft dar. In den ersten acht Wochen der Schwangerschaft führt eine Rötelninfektion in 90 % der Fälle zur Schädigung des Embryos. Mit fortschreitender Schwangerschaft sinkt das Risiko im mittleren Drittel der Schwangerschaft auf 25–30 %.[1] Mögliche Folgen einer Infektion des ungeborenen Kindes sind Spontanabort, Frühgeburt oder die klassische Kombination aus Fehlbildungen in Form von Herzfehlern (offener Ductus Botalli, Septumdefekte und Fallot-Tetralogie), Trübung der Linse der Augen (Katarakt) und Innenohrschwerhörigkeit. Dieses Vollbild, das auch Gregg-Syndrom genannt wird, entsteht bei Rötelninfektionen in der vierten Schwangerschaftswoche, wohingegen eine Infektion in der 20. Schwangerschaftswoche möglicherweise lediglich eine isolierte Taubheit auslöst.[1] Weitere in Frage kommende Schädigungen sind niedriges Geburtsgewicht, Blutungsneigung aufgrund verminderter Blutplättchenzahlen (Thrombozytopenische Purpura), Enzephalomeningitis, Leberentzündung, Vergrößerung von Leber und Milz, Herzmuskelentzündung (Myokarditis) oder verminderter Kopfumfang (Mikrozephalie)[1]. Daher gehört die Untersuchung auf Röteln zur Mutterschaftsvorsorge (siehe Röteln während der Schwangerschaft).
Untersuchung
Anders als bei anderen Kinderkrankheiten ist eine Diagnosestellung allein aufgrund der Krankheitszeichen immer unsicher. Röteln können mit anderen Infektionskrankheiten, die mit einem fleckigen Exanthem einhergehen, wie dem Drei-Tage-Fieber, Ringelröteln, Masern, Entero- oder Adenovirus-Infektionen, Mykoplasmen oder Scharlach verwechselt werden. Der direkte Nachweis des Rubellavirus in Rachenspülflüssigkeit, Urin oder anderen Sekreten ist in Speziallabors zwar grundsätzlich möglich, aber aufwändiger und in der Routinediagnostik nicht sinnvoll. Er ist speziellen Fragestellungen, beispielsweise bei angeborenen Infektionen vorbehalten.[1] Wenn wichtige Entscheidungen von der Diagnosestellung abhängen, beispielsweise bei Röteln-Verdacht bei einer Schwangeren, muss die Diagnose durch Untersuchung der Antikörper im Blut mittels Immunassay (ELISA) gestellt werden. Dabei gilt ein positiver Nachweis von IgM-Antikörpern als Hinweis, aber noch nicht als Nachweis einer Infektion. Dieser Test kann nämlich beispielsweise durch Kreuzreaktionen mit Antikörpern gegen andere Viren auch falsch-positiv ausfallen. Die Bestätigung einer Rötelninfektion kann durch Nachweis von Antikörpern gegen Rubellaviren im Hämagglutinationshemmtest (HHT) erfolgen. Dabei muss in zwei aufeinanderfolgenden Blutproben im Abstand von 14 Tagen ein Anstieg der Antikörpermenge (des Titers) um mindestens das Vierfache gefunden werden[1]. Eine weitere Bestätigungsmethode besteht im Nachweis durch den Hämolyse-im-Gel-Test. Beim Neugeborenen ist der Nachweis von Röteln-IgM im Rahmen der STORCH-Serologie beweisend für eine während der Schwangerschaft erworbene Rötelninfektion. Bei möglicher oder gesicherter Röteln-Infektion einer Schwangeren kann durch Nachweis des Rubellavirus mittels Zellkultur oder Polymerase-Kettenreaktion (PCR) im Fruchtwasser oder im Material einer Chorionzottenbiopsie, ab der 22. Schwangerschaftswoche auch im Fetalblut eine vorgeburtliche (pränatale) Infektion diagnostiziert werden. In der aktuellen Fassung des Infektionsschutzgesetzes sind der Verdacht, die Erkrankung und der Todesfall sowie der Nachweis des Erregers meldepflichtig.
Behandlung
Es existiert keine ursächliche Behandlung. Die symptomatische Therapie muss sich auf fiebersenkende Mittel oder entzündungshemmende Schmerzmittel bei Gelenkbeteiligung beschränken.[11] Erkrankte beziehungsweise deren Eltern sollten auf die mögliche Gefahr für empfängliche Schwangere hingewiesen werden.
Kinder mit während der Schwangerschaft erworbenen Röteln (Rötelnembryofetopathie) benötigen entsprechend der Ausprägung eine umfassende Betreuung, gegebenenfalls einschließlich Augen- oder Herzoperationen, Hörgeräteversorgung und Förderung beispielsweise durch Logopädie und Krankengymnastik.[11]
Vorbeugung
Expositionsprophylaxe
Erkrankte sollen bis sieben Tage nach Ausbruch des Hautausschlags Gemeinschaftseinrichtungen wie Schule oder Kindergarten meiden und auch dem Arbeitsplatz fernbleiben. Im Krankenhaus müssen Patienten mit Röteln isoliert werden. Dies gilt auch für Kinder mit angeborener Röteln-Infektion für die ersten sechs Lebensmonate, zumindest solange nicht mehrere Viruskulturen aus Nasenrachensekret und Urin negativ waren.[11]
Postexpositionsprophylaxe
Eine postexpositionelle passive Impfung mit spezifischen Immunglobulinen bei Schwangeren ist innerhalb von 72 Stunden nach Röteln-Kontakt möglich [1], schützt aber keineswegs sicher vor einer Infektion[11]. Bei Röteln-Kontakt im ersten Drittel der Schwangerschaft, fehlender Impfung und negativem Antikörperstatus in der Vorgeschichte soll sofort ein Antikörpertest durchgeführt werden. Bei nachgewiesener maternaler Infektion während einer Schwangerschaft hängt das Fehlbildungsrisiko des Kindes ganz entscheidend vom Stand der Schwangerschaft vom Infektionszeitpunkt ab; vor der vollendeten 12. SSW ist das Risiko des Vollbildes der Rötelnembryopathie hoch, danach sinkt es drastisch. Bei Infektionen nach der 12. SSW trägt das Kind meist nur Hörschäden davon [12][13].
Impfung
| Symptom/Erkrankung | Komplikationsrate bei Röteln-Erkrankung |
Komplikationsrate nach MMR-Impfung |
|---|---|---|
| Gelenkbeschwerden bei Erwachsenen |
40 bis 70 %, anhaltend | 1/10.000, meist kurz und schwach |
| Enzephalitis | 1/6000 | 0 |
| Verminderung der Blutplättchen | 1/3000 | 1/30 000 bis 1/50 000 |
| Rötelnembryofetopathie bei Infektion in der Schwangerschaft |
> 60 % | 0 |
Mit dem MMR-Impfstoff ist eine sichere Impfung gegen Masern, Mumps und Röteln verfügbar. In Deutschland wird sie durch die Ständige Impfkommission (STIKO) für alle Kinder ab dem zwölften Lebensmonat und alle Erwachsenen, bei denen keine IgG-Antikörper gegen Rötelnvirus nachweisbar sind (Seronegative), insbesondere bei Frauen, empfohlen (Impfkalender). Die Impfung vermittelt mit 95 % Effizienz eine lebenslange Immunität [2]. Über eine Wiederholungsimpfung, frühestens einen Monat nach erster Impfung, sollten Impflücken bei den verbliebenen 5 % geschlossen werden. In Österreich und der Schweiz sind die entsprechenden Impfempfehlungen gleichlautend.[16][17] Weltweit ist die Rötelnimpfung in 125 Ländern Bestandteil nationaler Impfprogramme, darunter auf dem gesamten amerikanischen, australischen und europäischen Kontinent (Stand 2007).[18] In Afrika und weiten Teilen Asiens ist sie noch nicht allgemein verbreitet, was dazu führt, dass mehr als zwei Drittel eines weltweiten Geburtsjahrgangs keine Impfung erhalten.
Fieber und lokale Impfreaktionen wie Rötung, Schmerzen und Schwellungen an der Injektionsstelle können wie bei allen Impfungen vorkommen und sind als harmlose Nebenwirkungen zu betrachten. Da es sich bei der MMR-Impfung um eine Impfung mit einem abgeschwächten Lebendimpfstoff handelt, können in seltenen Fällen abgeschwächte Formen der drei Infektionskrankheiten entstehen. In der Folge können sich ähnliche Symptome wie bei den Infektionskrankheiten entwickeln (s. Tabelle). Diese Auswirkungen sind üblicherweise leichter und kurzfristiger Natur. Obwohl also bekannte Nebeneffekte existieren, überwiegen die Vorteile gegenüber einer „natürlichen“ Infektion bei Weitem. Weitere mögliche Nebenwirkungen wurden immer wieder kontrovers diskutiert. Der Artikel MMR-Impfstoff enthält hierzu detailliertere Informationen.
Geschichte
Bis ins 18. Jahrhundert hinein wurden die Röteln nicht von anderen fieberhaften und mit einem Hautausschlag einhergehenden Infektionskrankheiten abgegrenzt. Die ersten Beschreibungen der klinischen Erscheinungen werden den deutschen Ärzten de Bergan und Orlow zugeschrieben, weswegen sie im englischen Sprachgebrauch auch als German Measles Eingang fanden.[19] Bis in das 19. Jahrhundert hinein gab es viele Mutmaßungen über die Verwandtschaft zwischen den Röteln einerseits und den Masern oder Scharlach andererseits, bis wiederum ein deutscher Arzt, George de Maton, 1814 die Rötheln endgültig als eigenständiges Krankheitsbild beschrieb. Die englische Bezeichnung Rubella wurde 1864 vom britischen Militärarzt Henry Veale eingeführt.[19] Anschließend wurden sie lange Zeit als harmlose Kinderkrankheit ohne Bedeutung eingeordnet.[20] Erst 1938 belegten Hiro und Tasaka die virale Ursache der Erkrankung.[19] Schließlich beschrieb Norman McAlister Gregg 1941 erstmals die schwerwiegenden Missbildungen bei Neugeborenen, deren Mütter während der Schwangerschaft Röteln gehabt hatten. Dies war der Ausgangspunkt für zahlreiche Forschungen, die 1962 zur Isolierung des Röteln-Virus[21] führten und 1966 in der allgemeinen Anwendung eines Impfstoffes mündeten.[20]
Literatur
- Marre, Reinhard; Mertens, Thomas; Trautmann, Matthias; Vanek, Ernst: Klinische Infektiologie. 1. Auflage. Urban & Fischer Verlag, München, Jena 2000
- Kayser, Fritz H.; Bienz, Kurt A.; Eckert, Johannes; Zinkernagel, Rolf M.: Medizinische Mikrobiologie: verstehen, lernen, nachschlagen. 9. Auflage. Thieme, Stuttgart, New York 1997
- Ocklitz, Hans W.; Mochmann, Hanspeter; Schneeweiß, Burkhard: Infektologie. 2. Auflage. VEB Verlag Volk und Gesundheit, Berlin 1977
Weblinks
- Röteln – Informationen des Robert-Koch-Instituts
Einzelnachweise
- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 1,11 1,12 Robert-Koch-Institut: Röteln (Rubella) RKI-Ratgeber Infektionskrankheiten – Merkblätter für Ärzte.
- ↑ 2,0 2,1 Kapitel Rubella (PDF; 475 kB). In: Epidemiology & Prevention of Vaccine-Preventable Diseases - „The Pink Book“, 12te Auflage, Public Health Foundation
- ↑ Infektionsschutzgesetz bei juris (PDF; 180 kB)
- ↑ 4,0 4,1 RKI: Epidemiologisches Bulletin 35/2004 (Volltext online, pdf)
- ↑ European Center for Disease Control and Prevention
- ↑ RKI: Epidemiologisches Bulletin 16/2012 (Volltext online, pdf)
- ↑ RKI: Infektionsepidemiologisches Jahrbuch, Anhang Jahresstatistik nach Bundesland. (Volltext online, pdf)
- ↑ Robertson SE, Featherstone DA, Gacic-Dobo M, Hersh BS: Rubella and congenital rubella syndrome: global update. In: Rev. Panam. Salud Publica. 14, Nr. 5, November 2003, S. 306–15. PMID 14870758.
- ↑ Dominguez G, Wang CY, Frey TK: Sequence of the genome RNA of rubella virus: evidence for genetic rearrangement during togavirus evolution. In: Virology. 177, Nr. 1, Juli 1990, S. 225–38. PMID 2353453.
- ↑ Bardeletti G, Kessler N, Aymard-Henry M: Morphology, biochemical analysis and neuraminidase activity of rubella virus. In: Arch. Virol.. 49, Nr. 2-3, 1975, S. 175–86. PMID 1212096.
- ↑ 11,0 11,1 11,2 11,3 Deutsche Gesellschaft für Pädiatrische Infektiologie e. V. (DGPI) (Hrsg.): Handbuch Infektionen bei Kindern und Jugendlichen. 5. Aufl. Georg Thieme, Stuttgart, New York 2009, ISBN 978-3-13-144715-9 Referenzfehler: Ungültiges
<ref>-Tag. Der Name „dgpi“ wurde mehrere Male mit einem unterschiedlichen Inhalt definiert. - ↑ Enders M, Biber M, Exler S. Masern, Mumps und Röteln in der Schwangerschaft. Mögliche Auswirkungen auf Mutter, Schwangerschaft und Fetus. Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz. 2007 Nov ;50(11):1393-1398.
- ↑ Miller E, Cradock-Watson JE, Pollock TM. Consequences of confirmed maternal rubella at successive stages of pregnancy. Lancet. 1982 Oct 9;2(8302):781-784.
- ↑ R.T. Chen: Vaccine risks: real, perceived and unknown. Vaccine 17/1999. S. 41–46
- ↑ C. Meyer, S. Reiter: Impfgegner und Impfskeptiker – Geschichte, Hintergründe, Thesen, Umgang. In: Bundesgesundheitsbl - Gesundheitsforsch - Gesundheitsschutz, Springer Medizin Verlag. 47, 2004, S. 1182–1188. doi:10.1007/s00103-004-0953-x. Abgerufen am 25. November 2012.
- ↑ Bundesministerium für Gesundheit, Familien und Jugend Österreichs (pdf)
- ↑ Schweizerischer Impfplan 2012, pdf
- ↑ WHO | Rubella and Congenital Rubella Syndrome (CRS). Abgerufen am 25. November 2008.
- ↑ 19,0 19,1 19,2 Lee JY, Bowden DS: Rubella virus replication and links to teratogenicity. In: Clin. Microbiol. Rev.. 13, Nr. 4, Oktober 2000, S. 571–87. PMID 11023958.
- ↑ 20,0 20,1 Max Micoud: Die ansteckenden Krankheiten: Klinische Beobachtung. In: Illustrierte Geschichte der Medizin, S. 4464 (vgl. GdMed Bd. 4, S. 2229) 1986
- ↑ Paul A. L. Lancaster: Gregg, Sir Norman McAlister (1892–1966) In: Australian Dictionary of Biography 1996; 14:325-327
| Bitte den Hinweis zu Gesundheitsthemen beachten! |
| Dieser Artikel wurde am 14. Dezember 2008 in dieser Version in die Liste der exzellenten Artikel aufgenommen. |
| Dieser Artikel basiert ursprünglich auf dem Artikel Röteln aus der freien Enzyklopädie Wikipedia und steht unter der Doppellizenz GNU-Lizenz für freie Dokumentation und Creative Commons CC-BY-SA 3.0 Unported. In der Wikipedia ist eine Liste der ursprünglichen Wikipedia-Autoren verfügbar. |